研究概要
本研究は日本のNICUでの抗菌薬適正使用を推進するために実施します。日本の多施設NICUに対して、既存の抗菌薬適正使用要素を複合した抗菌薬適正使用プログラムについて各施設の実施状況を確認すると共に、 同グロクラムが認知されることによる影響について、生後早期の極早産児または極低出生体重児に対する抗菌薬使用量の変化およびNICU入院中死亡率の推移を確認します。

研究背景
早産児は早発型敗血症(EOS)の罹患・死亡リスクが高く、抗菌薬が頻用されています。新生児への抗菌薬暴露は、多剤耐性菌保菌の増加に加え、異常な腸内細菌叢の形成に起因する短期・長期の健康障害の発症リスクとなります。
海外ガイドラインでは「全身状態が安定している生後早期の新生児において、36-48時間培養した血液培養が陰性ならば抗菌薬を中止する」等をはじめとした抗菌薬適正使用が推進されています。 しかしながら、我が国のNICUでの生後早期の抗菌薬使用状況には大きな施設間差があり、抗菌薬適正使用の普及を目的とした多施設での取り組みはいまだ行われていないことが問題として挙げられます。
複合的な抗菌薬適正プログラム
概略
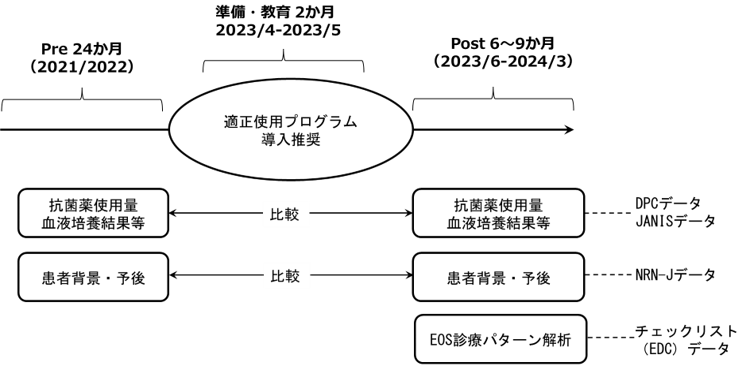
研究の対象者
研究の趣旨に賛同した総合周産期/地域周産期母子医療センターのNICUに入院した新生児のうち、
以下の適格基準と除外基準のいずれにも該当しない患者を研究対象者とする。
- 生後3日以降に入院した症例
- 分娩室死亡または致死的疾患等で積極的な救命治療を行わず看取りの方針を選択された症例
- 対象者の療育者から参加拒否の申し出があった症例 ※情報公開(オプトアウト) https://ccs.ncgm.go.jp/120/060/pdf/pdf_info/4580_info.pdfで拒否できる権利を保障しております。
収集情報
- 1) 診療録データ
-
入院月日、在胎期間(週日)、出生体重、アプガースコア(1分値/5分値)、性別、母体Lencki基準、出生に至った理由、前期破水≧18時間の有無、母体GBS保菌の有無、母体菌血症の有無、母体抗菌薬投与の有無、分娩様式(帝王切開の場合は理由)、初回採血時のBase excess値、入院時体温(℃)、NICU入院時の呼吸補助の有無、血液培養採取の有無、早発型敗血症に対する抗菌薬投与の有無、抗菌薬投与中の全身状態・血液培養結果・血液検査結果・抗菌薬中止/継続の判断、退院月日、退院時転帰、生後1週間以降の抗菌薬使用の有無、生後72時間以降に発症した敗血症の有無、重度脳室内出血(≧Pappile’s grade 3)の有無、壊死性腸炎(≧Bell’s grade2b)の有無、腸管穿孔(限局性腸管穿孔や胎便関連イレウスによる腸管穿孔をおこしたもの)の有無、慢性肺疾患(修正36週時点での酸素または呼吸サポート使用)の有無、耐性菌保菌の有無
上記について研究者または研究協力者が診療録よりEDCまたは紙ベースの入力フォームに転記する。 母体・出生時病歴、新生児アウトカム、死亡の有無については、参加施設の希望があればNRN-Jデータを二次利用する(特定NPO法人新生児臨床研究ネットワークからデータ二次利用申請を受理されている。理事長 楠田 聡)
- 2) DPCデータ
-
入院・退院月日、在胎期間・出生体重、入院中の血液培養実施状況、入院中の抗菌薬処方状況
上記について、研究者または研究協力者が手順に沿ってDPCデータ(様式1、様式4、EFファイル、Dファイル)を匿名化し、事務局に提出する。
- 3) JANISデータ
-
血液培養検出菌、多剤耐性菌保菌状況
上記について、研究者または研究協力者が手順書に沿ってJANISデータ(検査部門)をダウンロードし、事務局に提出する。
研究代表者
国立研究開発法人国立国際医療研究センター病院
AMR臨床リファレンスセンター 臨床疫学室長 松永展明
研究事務局
京都第一赤十字病院 新生児科 副部長
京都府立医科大学附属病院 小児科 大学院生 木下大介
